Evaluación de Tecnologías digitales en salud- ¿Cuáles atributos se deben valorar? ¿Cuál es la regulación aplicable?
La alerta reciente derivada del masivo ciberataque a la infraestructura tecnológica que provee servicios a más de 700 compañías públicas y privadas en países como Colombia, Chile y Argentina, ha puesto nuevamente en la agenda pública la importancia de fortalecer las acciones en ciberseguridad y proteger información sensible de los ciudadanos, las empresas y los estados.
El sector salud, que fue uno de los afectados en Colombia, no es ajeno a esta discusión. De allí la importancia de encontrar el balance adecuado entre maximizar los beneficios que ofrece la transformación tecnológica y asegurar altos estándares de calidad, eficiencia y seguridad para los ciudadanos.
Barreras por superar
El crecimiento en la inversión y desarrollo de tecnologías digitales en salud ha sido notable en los últimos años, sin embargo, aún persisten obstáculos que se deben considerar para lograr resultados tangibles en acceso, eficiencia y bienestar para la población (1–3):
- Alfabetización digital: Bajos niveles de conocimiento y entrenamiento de los profesionales en el campo de salud digital, así como limitada participación en los procesos de creación y adopción de nuevas herramientas.
- Acceso: Limitada disponibilidad de herramientas adecuadas a las necesidades y preferencias de los pacientes, sumado a otros determinantes para el uso de tecnologías como la edad, la ubicación geográfica, el nivel educativo o la disponibilidad de internet.
- Gobernanza: Falta de regulación y lineamientos integrados que aseguren el uso de herramientas confiables, con monitoreo y evaluación permanente de los riesgos y beneficios durante su desarrollo y adopción.
- Financiamiento: ¿Quien asume los costos de desarrollo y adopción de las tecnologías digitales en salud? ¿Cuál debe ser la cobertura de los sistemas de salud y las instituciones? ¿Es el costo una limitación para que los pacientes usen las tecnologías en salud? ¿Se pueden adoptar modelos de monetización utilizados en otros sectores?
Alfabetización digital
La implementación efectiva de tecnologías digitales requiere habilidades y conocimientos no solo por parte de los profesionales de salud sino también de los usuarios. Factores como la edad, las condiciones socio-económicas, la familiaridad y confianza en la herramienta tecnológica pueden ser determinantes del éxito durante la adopción y el uso adecuado de estas soluciones.
Existen diversos métodos para evaluar las habilidades y las capacidades en el uso de las tecnologías digitales, los servicios y los datos, siendo los más utilizados las encuestas o cuestionarios, i.e. Digital health technology literacy assessment questionnaire (DHLT-AQ), eHealth literacy scale (eHEALS). También se consideran de valor los grupos focales o las entrevistas para discutir con más detalle la percepción y necesidades de los usuarios (4,5). Considerar este tipo de herramientas es fundamental para facilitar acceso y equidad en la adopción de nuevas tecnologías digitales en salud que permita a los usuarios encontrar, entender y evaluar las aplicaciones.
Gobernanza
Para avanzar en este camino hacia la mayor disponibilidad y confiabilidad en el uso de tecnologías digitales, se han desarrollado diversos marcos de referencia en la gobernanza de datos y servicios de salud. Uno de ellos, Health data governance principles desarrollado por Transform health con un extenso grupo de expertos e instituciones de representación global, considera tres enfoques fundamentales: Proteger a las personas, Promover valor en salud y Priorizar la equidad (figura 1), en un esfuerzo de promover alineación y adopción por entidades de gobierno, academia, profesionales de las disciplinas involucradas y la población civil.
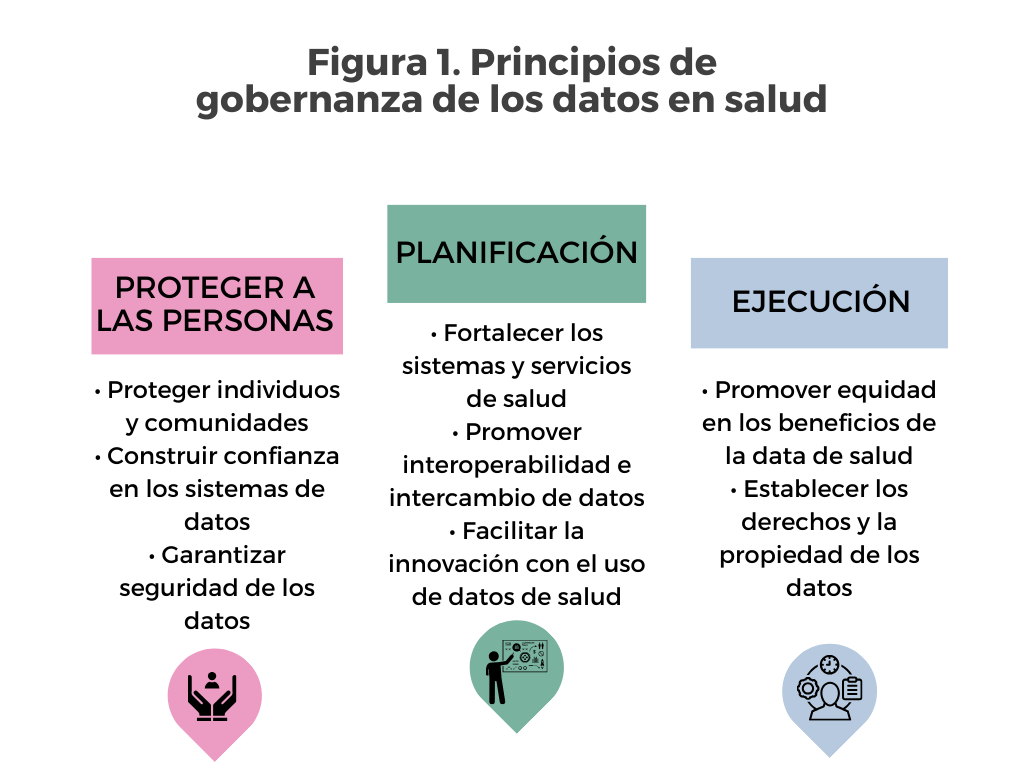
Fuente: Traducido y reproducido de healthdataprinciples.org (6)
De otro lado, para lograr una transformación digital efectiva, los gobiernos deben establecer una estrategia con visión de largo plazo y criterios claros de gobernanza que consideren las normas, los derechos de los usuarios, así como las responsabilidades y los riesgos en el uso de datos y sistemas de información en salud (7).
En Latinoamérica, Brasil se destaca por sus avances en regulación y articulación de actores públicos y privados en la búsqueda de mejores resultados en la adopción de tecnologías digitales en salud. Su estrategia digital en salud 2020 – 2028 provee un marco de referencia donde se establece la visión de largo plazo, el plan de acción y el plan de monitoreo y evaluación que asegure su revisión y actualización para servir a las necesidades de la población (8). No obstante, no existe un marco regulatorio único que consolide todos los lineamientos aplicables a la implementación de esta estrategia en Brasil.
En Colombia, marcos regulatorios de diferentes agencias y organismos definen obligaciones o criterios aplicables – aunque no necesariamente específicos – para el desarrollo de tecnologías digitales para el sector salud (Tabla 1), y que por tanto deben ser observadas durante el proceso de diseño, desarrollo y evaluación (9,10).
Tabla 1. Marco regulatorio en Colombia aplicable al desarrollo de tecnologías digitales en salud.
| Tópico | Agente emisor | Tipo de regulación | Observaciones |
| Privacidad y protección de datos personales | Congreso de Colombia | Ley Estatutaria 1581 de 2012 | Datos de salud son “sensibles” y cuentan con protección especial |
| Presidencia de la República | Decreto 1377 de 2013 | Disposiciones generales para la protección de datos personales | |
| Ministerio de Salud y Protección social | Política de privacidad y protección de datos personales, septiembre 2021 | Lineamientos para el registro, custodia, protección, entrega, modificación y/o supresión de los datos personales recolectados por el Ministerio y sus agentes | |
| TIC y Ciber-seguridad | Congreso de Colombia | Ley 1341 de 2009 | Regula las TIC, gobernanza digital y autoriza a MinTIC par a desarrollar telemedicina |
| Ministerio de Tecnologías de la Información y Comunicaciones | Resolución 500 de 2021 – Política de gobierno digital | Lineamientos sobre seguridad digital y privacidad de la información | |
| Salud digital | Congreso de Colombia | Ley 1419 de 2010 | Lineamientos para implementar telesalud, telemedicina y teleeducación |
| Ministerio de Salud y Protección social | Resolución 2654 de 2019 | Establece los parámetros para la práctica de telemedicina, incluyendo habilitación, consentimiento informado y protección de datos | |
| Congreso de Colombia | Ley 2015 de 2020 | Regula componentes de la historia clínica electrónica e interoperabilidad | |
| Ministerio de Salud y MinTIC | Resolución 866 de 2021 | ||
| Derechos de Propiedad intelectual | Comisión de la Comunidad Andina | Decisión 486 del 14 de septiembre del 2000 | Derecho de marca cuyo signo es registrado ante la Superintendencia de industria y Comercio |
| Congreso de Colombia / Comunidad Andina de Naciones | Ley 23 de 28 de enero 1982 / Decisión 351 de la Comisión del Acuerdo de Cartagena | Derechos de autor, protege software similar a obras literarias | |
| Comunidad Andina de Naciones | Decisión Andina 486 del 2000 / Decisiones de la SIC | Derecho de patentes cuando se demuestra que un programa de ordenador ofrece soluciones de carácter técnico de forma inventiva | |
| Innovación y emprendimiento | Congreso de Colombia | Ley 2069 de 2020 | Marco regulatorio para propiciar el emprendimiento y el crecimiento, consolidación y sostenibilidad de las empresas |
| Ministerio de TIC | Decreto 1732 de 2021 | Crea los ambientes especiales de vigilancia y control o sandbox regulatorio |
Fuente: Elaboración propia, adaptado de Jiménez et al.,2022 y Rodríguez et al.,2018. TIC: Tecnologías de la Información y Comunicaciones
Otro aspecto relevante es la existencia de estándares y parámetros para garantizar interoperabilidad, es decir, el intercambio electrónico de datos que son capturados y registrados en los sistemas de atención médica. Uno de los más reconocidos y aplicados en Colombia es el conjunto de estándares Health Level seven (HL-7) y su especificación más reciente FHIR (Fast Healthcare Interoperability Resource) -de código abierto y gratuito-, que permite la conexión de varias aplicaciones a un sistema operativo básico, para facilitar que la información de los pacientes esté disponible mientras “navegan” por los diferentes puntos de atención en el sistema de salud.
Dado que en Colombia aún no se cuenta con reglamentación específica en el INVIMA para establecer el alcance y la ruta de aprobación de tecnologías digitales, vale la pena observar la experiencia de Brasil, donde ANVISA definió los criterios de aprobación para comercialización de software como dispositivo médico / software como servicio, bajo el marco de evaluación de dispositivos médicos, siguiendo el ejemplo de avance regulatorio en esta materia en Estados Unidos y Europa (11,12).
La Resolución 657 de 2022 de ANVISA (11) establece los requisitos y contenidos del dossier técnico que debe ser presentado por el solicitante, según la clase de riesgo (I – IV). Además, excluye del ámbito de aplicación software relacionado con los siguientes usos:
- Bienestar
- Producto no regulado por la Agencia
- Gerenciamiento administrativo o financiero de servicios de salud
- Procesamiento de datos médicos demográficos o epidemiológicos sin finalidad clínica diagnóstica o terapéutica
- Dispositivos médicos bajo régimen de vigilancia sanitaria
¿Cómo evaluar las intervenciones digitales en salud?
Para los desarrolladores de tecnologías digitales en salud, es todo un reto demostrar valor para el bienestar y cuidado de la salud. Por un lado, se enfrentan al ritmo acelerado y alta competitividad que existe a la hora de crear nuevas soluciones y por el otro, a la dinámica de creación y maduración de cada solución, que tiende a ser un proceso iterativo, con actualizaciones y mejoras con el uso y el paso del tiempo. En esto difieren de manera importante de los parámetros para evaluación de medicamentos o dispositivos que son altamente estandarizados y específicos (13).
El otro aspecto relevante es la diferenciación de uso como una tecnología de intervención médica (diagnóstico, tratamiento o monitoreo activo) vs aquellas dirigidas “al consumidor”, es decir destinadas a ofrecer información, educación o facilitar procesos de atención. Sobre las primeras es donde recae mayor responsabilidad de regulación, incluso el cumplimento de parámetros de efectividad comparativa soportada en estudios clínicos, adicional a los requerimientos en seguridad, privacidad de datos, funcionalidad, calidad e interoperabilidad, etc. Estos procesos de valoración permiten adicionalmente definir los parámetros para la cobertura y reembolso de estas tecnologías por parte de los sistemas de salud (14,15).
¿Cuáles países han establecido mecanismos de evaluación de terapéuticos digitales?
En los últimos años las agencias regulatorias y de evaluación de tecnologías de países desarrollados han dado pasos importantes en la definición de mecanismos y criterios para evaluar tecnologías digitales de intervención y aplicaciones móviles, la mayoría bajo el amparo de la regulación existente para dispositivos médicos.
Bélgica y Alemania se destacan en los avances para acelerar los procesos de acceso a mercado y reembolso, y promueven la creación de directorios de aplicaciones certificadas disponibles para consulta pública (Figura 2). En general se observan procesos centralizados, con mecanismos de evaluación acelerada (“fast-track”) y revisiones posteriores a la implementación, bajo el liderazgo conjunto de agencias regulatorias y agencias de evaluación de tecnologías. Estos procesos también cuentan con la participación de otros actores de interés como sociedades científicas, representantes de la industria de tecnologías de la información (IT), desarrolladores de tecnologías y de los consumidores, entre otros. La realización y presentación de estudios económicos varía según el tipo de uso, impacto económico de su adopción y riesgo para el pagador, con lo cual algunas tecnologías requieren generar evidencia clínica y económica previo a su comercialización (15,16).
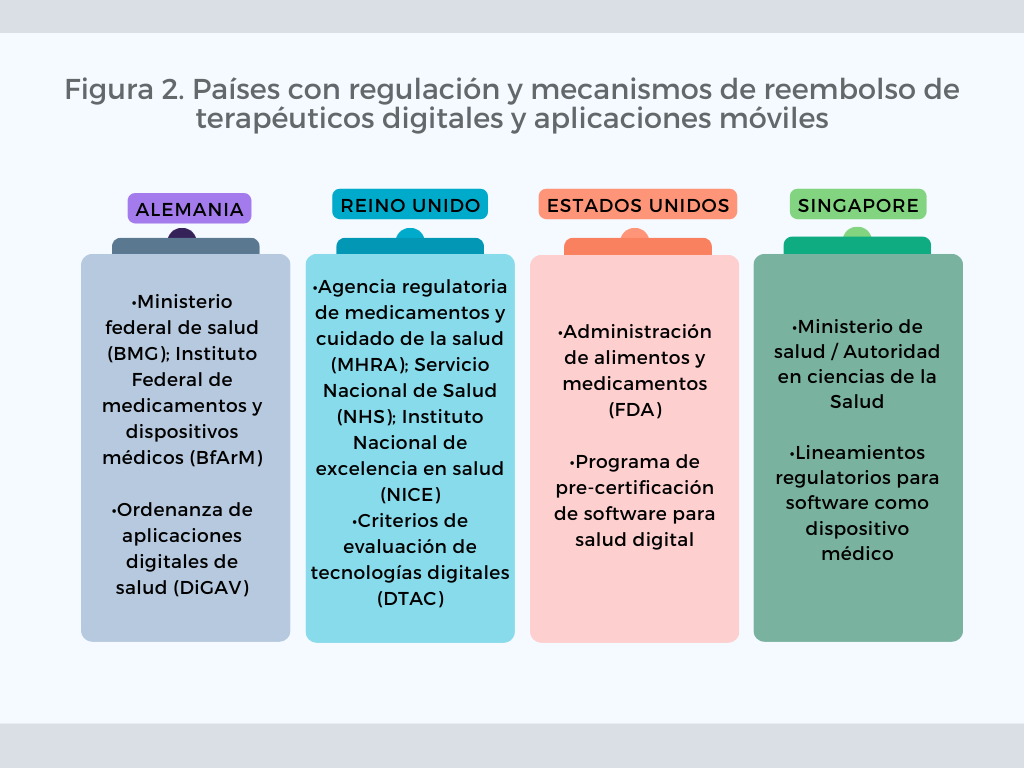
Fuente: Elaboración propia. Adaptado de Yan, K et al (2021); Essén, A et al. (2022). BMG: Federal Ministry of Health; BfArM: Federal Institute for Drugs and Medical devices; DiGAV: Digital health applications ordinance; MHRA: Medicines and Healthcare Regulatory Agency; NHS: National health service; NICE: National Institute of Health and Care Excellence; DTAC: Digital Technology Assessment Criteria; FDA: Food and Drug Administration.
¿Cuáles son los criterios de evaluación?
Como hemos visto, existe un número creciente de regulaciones y marcos de referencia para evaluar tecnologías digitales, con diferentes niveles de articulación entre los agentes de los diferentes sistemas de salud. En general, se busca regular aquellas consideradas de intervención o dispositivos médicos determinando su finalidad de uso, el nivel de riesgo al que se exponen los pacientes, así como los criterios de valor y preferencias que faciliten la toma de decisiones sobre su adopción, prescripción y cobertura por los sistema de salud (14,17,18).
Diversas organizaciones han participado en la construcción de dominios y criterios de evaluación de aplicaciones digitales, como la OMS, la Organización para Revisión y Cuidado de Aplicaciones de Salud (ORCHA), el Colegio Americano de Médicos (ACP), la Asociación Americana de Telemedicina (ATA) así como, grupos académicos y de investigación que compilan la visión de profesionales de salud, pacientes y desarrolladores de tecnologías (figura 3) (2,14,17,19,20).

Fuente: Elaboración propia con ejemplos de los dominios y criterios más comunes según lo reportado por Digital Health Assessment Framework (2023); Haig, M (2023), Uncovska,M (2023), ORCHA (2022), ICER-PHTI (2023). AAA: Acuerdos de acceso administrado
Todos estos mecanismos y diversos criterios de evaluación se convierten en un referente de gran importancia para los actores en los sistemas de salud en América Latina, para convocar acciones multisectoriales que generen sinergias, y así lograr una adopción rápida asegurando ganancias en cobertura y equidad, ofreciendo mejores beneficios a los pacientes con los menores riesgos posibles y optimizando el uso de los recursos.
1. The digital divide among caregivers of pediatric patients aged 0 to 12 years. Design and validation of a questionnaire. Arch Argent Pediatr [Internet]. 2023 Dec 1 [cited 2023 Aug 30];121(6). Available from: https://www.sap.org.ar/docs/publicaciones/archivosarg/2023/v121n6a08e.pdf
2. Orchahealth [Internet]. [cited 2023 Sep 11]. The organisation for the Review of Care and Health Apps. Available from: https://orchahealth.com
3. Antoja G, Ribera J, Mur J. ¿Cómo financiar las apps de Salud? [Internet]. Center for Research in Healthcare Innovation Management, IESE Business School – University of Navarra; 2019. Available from: https://media.iese.edu/research/pdfs/ST-0528.pdf
4. Yoon J, Lee M, Ahn JS. Development and validation of Digital Health Technology Assessment Questionnaire. J Med Syst. 2022;46(13).
5. Faux-Nightingale A, Philp F, Chadwick D, Singh B, Pandyan A. Available tools to evaluate digital health literacy and engagement with eHealth resources: A scoping review. Heliyon. 2022 Aug;8(8):e10380.
6. Health data governance principles [Internet]. [cited 2023 Sep 20]. Available from: https://healthdataprinciples.org/principles
7. Carnicero J, Serra P. Gobernanza de la salud digital: El arte de la transformación de los sistemas de salud [Internet]. 2020th ed. Inter-American Development Bank; 2020 Sep [cited 2023 Aug 30]. Available from: https://publications.iadb.org/es/node/28855/
8. Brazil Ministry of Health. Brazilian National Digital Health Strategy 2020-2028 [Internet]. Ministry of health; 2020 [cited 2023 Sep 23]. Available from: https://bvsms.saude.gov.br/bvs/publicacoes/strategy_health_digital_brazilian.pdf
9. Jimenez-M MB, Guerrero-C J, González-Uribe C. Salud Digital y Derechos Digitales en Colombia. Univ Los Andes – Colev [Internet]. 2022 Nov; Available from: https://colev.uniandes.edu.co/images/documentos/IP-DRAG-ESP-Colombia-FINAL.pdf
10. Rodríguez Gómez AE, Rojas Rosario HA. Aplicaciones móviles: protección jurídica desde el ámbito de la propiedad intelectual en Colombia. Rev Prop Inmater. 2018 Dec 6;(26):117–42.
11. Agência Nacional De Vigilância Sanitária. RESOLUÇÃO DE DIRETORIA COLEGIADA – RDC No 657, DE 24 DE MARÇO DE 2022 [Internet]. RDC 657 de 2022 Mar 24, 2022. Available from: https://www.in.gov.br/en/web/dou/-/resolucao-de-diretoria-colegiada-rdc-n-657-de-24-de-marco-de-2022-389603457
12. Colloud S, Metcalfe T, Askin S, Belachew S, Ammann J, Bos E, et al. Evolving regulatory perspectives on digital health technologies for medicinal product development. Npj Digit Med. 2023 Mar 29;6(1):56.
13. Halminen O, Chen A, Tenhunen H, Lillrank P. Demonstrating the value of digital health: Guidance on contextual evidence gathering for companies in different stages of maturity. Health Serv Manage Res. 2021 Feb;34(1):13–20.
14. Uncovska M, Freitag B, Meister S, Fehring L. Rating analysis and BERTopic modeling of consumer versus regulated mHealth app reviews in Germany. Npj Digit Med. 2023 Jun 21;6(1):115.
15. Yan K, Balijepalli C, Druyts E. The Impact of Digital Therapeutics on Current Health Technology Assessment Frameworks. Front Digit Health. 2021 Jun 9;3:667016.
16. Essén A, Stern AD, Haase CB, Car J, Greaves F, Paparova D, et al. Health app policy: international comparison of nine countries’ approaches. Npj Digit Med. 2022 Mar 18;5(1):31.
17. Haig M, Main C, Chávez D, Kanavos P. A Value Framework to Assess Patient-Facing Digital Health Technologies That Aim to Improve Chronic Disease Management: A Delphi Approach. Value Health. 2023 Jun;S1098301523030255.
18. Gensorowsky D, Witte J, Batram M, Greiner W. Market access and value-based pricing of digital health applications in Germany. Cost Eff Resour Alloc. 2022 Dec;20(1):25.
19. Digital Health Assessment Framework [Internet]. [cited 2023 Sep 29]. Digital health assessment framework. Available from: https://dhealthframework.org/
20. ICER. ICER-PHTI Assessment Framework for Digital Health Technologies [Internet]. ICER; 2023 [cited 2023 Sep 29]. Available from: https://phti.com/wp-content/uploads/sites/3/2023/09/ICER-PHTI-Assessment-Framework-for-Digital-Health-Technologies.pdf